Добро пожаловать на наш портал
На нашем сайте ежедневно публикуются десятки качественных и свежих материалов, которые Вы можете скачать абсолютно бесплатно. Рекомендуем Вам добавить Наш сайт в закладки, а также подписаться на RSS ленту, чтобы не пропускать интересных новостей.




Перевести страницуМини-чатОпрос |
IV. Органическая химия 2 часть
Просмотров: 2082
18.01.2012
9. ФенолыФенолами называются производные аренов, в которых один или несколько атомов водорода ароматического кольца замещены на гидроксильные группы. По числу гидроксильных групп в ароматическом кольце различают одно– и многоатомные (двух– и трехатомные) фенолы. Для большинства фенолов используются тривиальные названия. Структурная изомерия фенолов связана с различным положением гидроксильных групп. 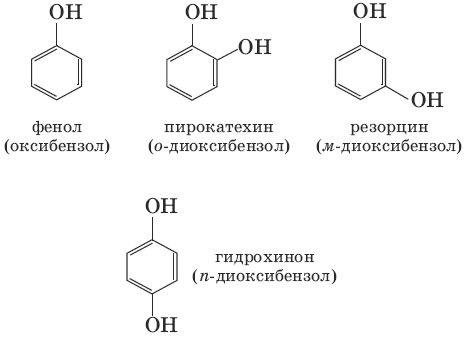
Способы получения фенолов1. С6Н5Cl + NaOH(p, 340°C) → С6Н5OH + NaCl (щелочной гидролиз галогеноуглеводородов) 2. (кумольный способ получения) 
3. C6H5SO3Na + NaOH (300–350°C) → С6Н5OH + Na2SO3 (щелочное плавление солей ароматических сульфоновых кислот) Химические свойства феноловФенолы в большинстве реакций по связи О—Н активнее спиртов, поскольку эта связь более полярна за счет смещения электронной плотности от атома кислорода в сторону бензольного кольца (участие непо-деленной электронной пары атома кислорода в системе л-сопряжения). Кислотность фенолов значительно выше, чем спиртов. Для фенолов реакции разрыва связи С—О не характерны. Взаимное влияние атомов в молекуле фенола проявляется не только в особенностях поведения гидроксигруппы, но и в большей реакционной способности бензольного ядра. 
Гидроксильная группа повышает электронную плотность в бензольном кольце, особенно в орто– и пара-положениях (+М-эффект OH-группы). Для обнаружения фенолов используется качественная реакция с хлоридом железа(III). Одноатомные фенолы дают устойчивое сине-фиолетовое окрашивание, что связано с образованием комплексных соединений железа. 1. 2С6Н5OH + 2Na → 2C6H5ONa + Н2 (так же, как и этанол) 2. С6Н5OH + NaOH → C6H5ONa + H2O (в отличие от этанола) C6H5ONa + Н2O + CO2 → С6Н5OH + NaHCO3 (фенол более слабая кислота, чем угольная) 3. 
Фенолы не образуют сложные эфиры в реакциях с кислотами. Для этого используются более реакционноспособные производные кислот (ангидриды, хлорангидриды). 4. С6Н5OH + CH3CH2OH →NaOH→ С6Н5OCH2CH3 + NaBr (О-алкилирование) 5. 
(взаимодействие с бромной водой, качественная реакция) 6.(нитрование разб. HNO3, при нитрировании конц. HNO3 образуется 2,4,6-тринитрофенол) 
7. nC6H5OH + nCH2O → nH2O + (—C6H3OH—CH2—)n (поликонденсация, получение фенолформальдегидных смол) 10. Альдегиды и кетоныАльдегидами называются соединения, в которых карбонильная группа 
соединена с углеводородным радикалом и атомом водорода, а кетонами – карбонильные соединения с двумя углеводородными радикалами. 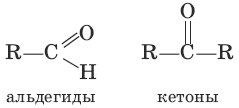
Систематические названия альдегидов строят по названию соответствующего углеводорода с добавлением суффикса –аль. Нумерацию цепи начинают с карбонильного атома углерода. Тривиальные названия производят от тривиальных названий тех кислот, в которые альдегиды превращаются при окислении: Н2С=O – метаналь (муравьиный альдегид, формальдегид); CH3CH=O – этаналь (уксусный альдегид). Систематические названия кетонов несложного строения производят от названий радикалов с добавлением слова «кетон». В более общем случае название кетона строится по названию соответствующего углеводорода и суффикса –он; нумерацию цепи начинают от конца цепи, ближайшего к карбонильной группе. Примеры: CH3—CO—CH3 – диметилкетон (пропанон, ацетон). Для альдегидов и кетонов характерна структурная изомерия. Изомерия альдегидов: а) изомерия углеродного скелета, начиная с С4; б) межклассовая изомерия. Изомерия кетонов: а) углеродного скелета (с С5); б) положения карбонильной группы (с С5); в) межклассовая изомерия. Атомы углерода и кислорода в карбонильной группе находятся в состоянии sp2-гибридизации. Связь С=O сильно полярна. Электроны кратной связи С=O смещены к электроотрицательному атому кислорода, что приводит к появлению на нем частичного отрицательного заряда, а карбонильный атом углерода приобретает частичный положительный заряд. Способы получения альдегидов и кетонов1. а) (дегидрирование, окисление первичных спиртов) 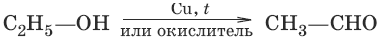
б) (дегидрирование, окисление вторичных спиртов) 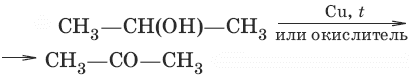
2. а) CH3CH2CHCl2 + 2NaOH →в воде→ CH3CH2CHO + 2NaCl + H2O (гидролиз дигалогенопроизводных) б) CH3СCl2CH3 + 2NaOH →в воде→ CH3COCH3 + 2NaCl + H2O 3. (гидратация алкинов, реакция Кучерова) 

4. (окисление этилена до этаналя) 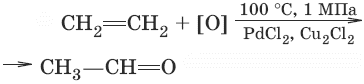
(окисление метана до формальдегида) CH4 + O2 →400–600 °C, NO→ H2C=O + H2O Химические свойства альдегидов и ке-тоновДля карбонильных соединений характерны реакции различных типов: а) присоединение по карбонильной группе; б) восстановление и окисление; в) конденсация; д) полимеризация. 1. (присоединение циановодородной кислоты, образование гидроксинитрилов) 
2. (присоединение гидросулбфита натрия) 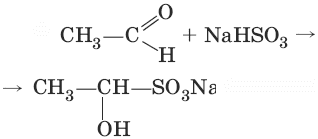
3. (восстановление) 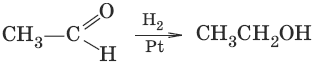
4. (образование полуацеталец и ацеталей) 
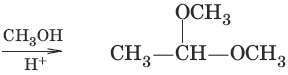
5. (взаимодействие с гидроксоламином, образование оксима ацетальдегида) 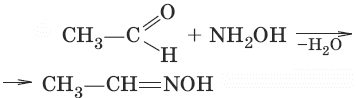
6. (образование дигалогенопроизводных) 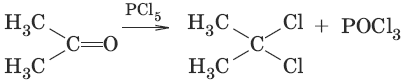
7. (α-галогенирование в присутствии OH¯) 
8. (албдольная конденсация) 
9. R—CH=O + Ag2O →NH3→ R—COOH + 2Ag↓ (окисление, реакция «серебряного зеркала») R—CH=O + 2Cu(OH)2 → R—COOH + Cu2O↓, + 2H2O (красный осадок, окисление) 10. (окисление кетонов, жесткие условия) 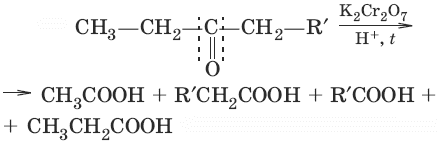
11. nCH2=O → (—CH2—O—)n параформ n = 8—12 (полимеризация) 11. Карбоновые кислоты и их производныеКарбоновыми кислотами называются органические соединения, содержащие одну или несколько карбоксильных групп —COOH, связанных с углеводородным радикалом. По числу карбоксильных групп кислоты подразделяются на: одноосновные (монокарбоновые) CH3COOH (уксусная), многоосновные (дикарбоновые, трикарбоновые и т. д.). По характеру углеводородного радикала различают кислоты: предельные (например, CH3CH2CH2COOH); непредельные (CH2=CH(—COOH); ароматические (С6Н5COOH). Систематические названия кислот даются по названию соответствующего углеводорода с добавлением суффикса –овая и слова «кислота»: HCOOH – метановая (муравьиная) кислота, CH3COOH – этановая (уксусная) кислота. Для карбоновых кислот характерная структурная изомерия: а) изомерия скелета в углеводородном радикале (начиная с С4); б) межклассовая изомерия, начиная с С2. Возможна цис-транс-изомерия в случае непредельных карбоновых кислот. Электронная плотность π-связи в карбонильной группе смещена в сторону атома кислорода. Вследствие этого у карбонильного углерода создается недостаток электронной плотности, и он притягивает к себе неподеленные пары атома кислорода гидроксильной группы, в результате чего электронная плотность связи О—Н смещается в сторону атома кислорода, водород становится подвижным и приобретает способность отщепляться в виде протона. 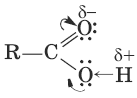
В водном растворе карбоновые кислоты диссоциируют на ионы: R—COOH ↔ R—COО¯ + Н+ Растворимость в воде и высокие температуры кипения кислот обусловлены образованием межмолекулярных водородных связей. Способы получения карбоновых кислот1. CH3—СCl3 + 3NaOH → CH3—COOH + 3NaCl + Н2O (гидролиз тригалогенопроизводных) 2. R—CHO + [О] → R—COOH (окисление альдегидов и кетонов) 3. CH3—CH=CH2 + CO + Н2O/Н+ →Ni, р, t→ CH3—CH2—CH2—COOH (оксосинтез) 4. CH3C≡N + 2Н2O/ Н+ → CH3COOH + NH4 (гидролиз нитрилов) 5. CO + NaOH → HCOONa; 2HCOONa + H2SO4 → 2HCOOH + Na2SO4 (получение HCOOH) Химические свойства карбоновых кислот и их производныхКарбоновые кислоты проявляют высокую реакционную способность и вступают в реакции с различными веществами, образуя разнообразные соединения, среди которых большое значение имеют функциональные производные: сложные эфиры, амиды, нитрилы, соли, ангидриды, гало-генангидриды. 1. а) 2CH3COOH + Fe → (CH3COO)2Fe + Н2 (образование солей) б) 2CH3COOH + MgO → (CH3COO)2Mg + Н2O в) CH3COOH + KOH → CH3COОК + Н2O г) CH3COOH + NaHCO3 → CH3COONa + CO2 + Н2O CH3COONa + H2O ↔ CH3COOH + NaOH (соли карбоновых кислот гидролизуются) 2. (образование вложных эфиров) 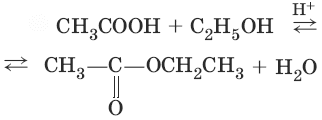
(омыление вложного эфира) 
3. (получение хлорангидридов кислот) 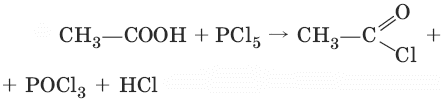
4. (разложение водой) 
5. CH3—COOH + Cl2 →hv→ Cl—CH2—COOH + HCl (галогенирование в α-положение) 6. HO—CH=O + Ag2O →NH3→ 2Ag + Н2CO3 (Н2O + CO2) (особенности HCOOH) HCOOH →t→ CO + Н2O 12. ЖирыЖиры – сложные эфиры глицерина и высших одноатомных карбоновых кислот. Общее название таких соединений – триглицериды. В состав природных триглицеридов входят остатки насыщенных кислот (пальмитиновой С15Н31COOH, стеариновой С17Н35COOH) и ненасыщенных (олеиновой С17Н33COOH, линолевой С17Н31COOH). Жиры состоят главным образом из триглицеридов предельных кислот. Растительные жиры – масла (подсолнечное, соевое) – жидкости. В состав триглицеридов масел входят остатки непредельных кислот. 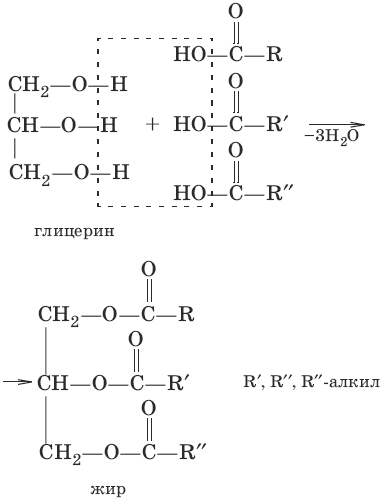
Жирам как сложным эфирам свойственна обратимая реакция гидролиза, катализируемая минеральными кислотами. При участии щелочей гидролиз жиров происходит необратимо. Продуктами в этом случае являются мыла – соли высших карбоновых кислот и щелочных металлов. Натриевые соли – твердые мыла, калиевые – жидкие. Реакция щелочного гидролиза жиров называется также омылением. 
13. АминыАмины – органические производные аммиака, в молекуле которого один, два или три атома водорода замещены на углеводородные радикалы. В зависимости от числа углеводородных радикалов различают первичные RNH2, вторичные R2NH, третичные R3N амины. По характеру углеводородного радикала амины подразделяются на алифатические (жирные), ароматические и смешанные (или жирноароматические). Названия аминов в большинстве случаев образуют из названий углеводородных радикалов и суффикса –амин. Например, CH3NH 2 – метиламин; CH3—CH2—NH2 – этиламин. Если амин содержит различные радикалы, то их перечисляют в алфавитном порядке: CH3—CH2—NH—CH3 – ме-тилэтиламин. Изомерия аминов определяется количеством и строением радикалов, а также положением аминогруппы. Связь N—Н является полярной, поэтому первичные и вторичные амины образуют межмолекулярные водородные связи. Третичные амины не образуют ассоциирующих водородных связей. Амины способны к образованию водородных связей с водой. Поэтому низшие амины хорошо растворимы в воде. С увеличением числа и размеров углеводородных радикалов растворимость аминов в воде уменьшается. Способы получения аминов1. R—NO2 + 6[Н] → R—NH2 + 2H2O (восстановление нитросоединений) 2. NH3 + CH3I → [CH3N+H3]I¯ →NH3→ CH3NH 2 + NH 4I (алкилирование аммиака) 3. а) С6Н5—NO2 + 3(NH4)2S → С6Н5—NH2 + 3S + 6NH3 + 2H2O (реакция Зинина) б) С6Н5—NO2 + 3Fe + 6HCl → С6Н5—NH2 + 3FeCl2 + 2Н2O (восстановление нитросоединений) в) С6Н5—NO2 + ЗН2 →катализатор, t→ C6H5—NH 2 + 2Н2O 4. R—C≡N + 4[H] → RCH2NH2 (восстановление нитрилов) 5. ROH + NH3 →Al2O3,350 °C→ RNH2 + 2H2O (получение низших алкиламинов С2—С4) Химические свойства аминовАмины имеют сходное с аммиаком строение и проявляют подобные ему свойства. Как в аммиаке, так и в аминах атом азота имеет неподеленную пару электронов. Для аминов характерны ярко выраженные основные свойства. Водные растворы алифатических аминов проявляют щелочную реакцию. Алифатические амины – более сильные основания, чем аммиак. Ароматические амины являются более слабыми основаниями, чем аммиак, поскольку не-поделенная электронная пара атома азота смещается в сторону бензольного кольца, вступая в сопряжение с его π-электронами. 
На основность аминов влияют различные факторы: электронные эффекты углеводородных радикалов, пространственное экранирование радикалами атома азота, а также способность образующихся ионов к стабилизации за счет сольватации в среде растворителя. В результате донорного эффекта алкильных групп основность алифатических аминов в газовой фазе (без растворителя) растет в ряду: первичные < вторичные < третичные. Основность ароматических аминов зависит также от характера заместителей в бензольном кольце. Электроноакцепторные заместители (—F, —Cl, —NO2 и т. п.) уменьшают основные свойства ариламина по сравнению с анилином, а электронодонорные (алкил R—, —OCH3, —N(CH3)2 и др.), напротив, увеличивают. 1. CH3—NH 2 + Н2O → [CH3—NH3]OH (взаимодействие с водой) 2. (CH 3)2NH + HCl → [(CH3)2NH2]Cl хлорид диметиламмония (взаимодействие с кислотами) [(CH 3)2NH 2]Cl + NaOH → (CH 3)2NH + NaCl + H2O (взаимодействие солей аминов со щелочами) 3. 
(ацителирование, с третичными аминами не идет) 4. R—NH2 + CH3I → [CH3N+H2R]I¯ →NH3→ CH3NHR + NH4I (алкилирование) 5. Взаимодействие с азотистой кислотой: строение продуктов реакции с азотистой кислотой зависит от характера амина. Поэтому данная реакция используется для различия первичных, вторичных и третичных аминов. а) R—NH2 + HNO2 → R—OH + N2 + H2O (первичные жирные амины) б) С6Н5—NH2 + NaNO2 + HCl → [С6Н5—N≡N]+Cl¯ – соль диазония (первичные ароматические амины) в) R2NH + Н—О—N=O → R2N—N=O (N-нитрозамин) + Н2O (вторичные жирные и ароматические амины) г) R3N + Н—О—N=O → при низкой температуре нет реакции (третичные жирные амины) д) 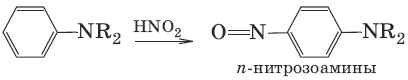
(третичные ароматические амины) Свойства анилина. Для анилина характерны реакции как по аминогруппе, так и по бензольному кольцу. Бензольное кольцо ослабляет основные свойства аминогруппы по сравнению с алифатическими аминами и аммиаком, но под влиянием аминогруппы бензольное кольцо становится более активным в реакциях замещения по сравнению с бензолом. C6H5—NH2 + HCl → [C6H5—NH3]Cl = C6H5NH2 • HCl C6H5NH2 • HCl + NaOH → C6H5NH2 + NaCl + H2O C6H5NH2 + CH3I →t→ [C6H5NH2CH3]+I¯ 
14. АминокислотыАминокислотами называются гетеро-функциональные соединения, молекулы которых содержат одновременно аминогруппу и карбоксильную группу. В зависимости от взаимного расположения амино– и карбоксильной групп аминокислоты подразделяют на α-, β-, γ– и т. д. По ИЮПАК, для наименования аминокислот группу NH2— называют приставкой амино-, указывая цифрой номер углеродного атома, с которым она связана, а затем следует название соответствующей кислоты. 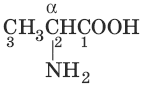
2-аминопропановая кислота (α-аминопропановая, α-аланин)
3-аминопропановая кислота (β-аминопропановая, β-аланин)
6-аминогексановая кислота (ε-аминокапроновая)По характеру углеводородного радикала различают алифатические (жирные) и ароматические аминокислоты. Изомерия аминокислот зависит от строения углеродного скелета, положения аминогруппы по отношению к карбоксильной группе. Для аминокислот характерна еще оптическая изомерия. Способы получения аминокислот1. (аммонолиз галогенокислот) 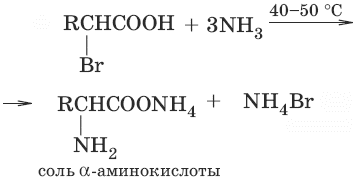
2. CH2=CH—COOH + NH3 → H2N—CH2—CH2—COOH (присоединение аммиака к α, β-непредельным кислотам) 3. 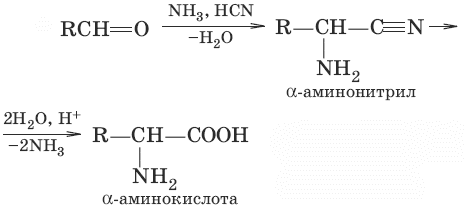
(действие HCN и NH3 на альдегиды или кетоны) 4. Гидролиз белков под влиянием ферментов, кислот или щелочей. 5. Микробиологический синтез. Химические свойства аминокислотАминокислоты проявляют свойства оснований за счет аминогруппы и свойства кислот за счет карбоксильной группы, т. е. являются амфотерными соединениями. В кристаллическом состоянии и в среде, близкой к нейтральной, аминокислоты существуют в виде внутренней соли – дипо-лярного иона, называемого также цвиттер-ион H3N+—CH2—COO¯. 1. H2N—CH2—COOH + HCl → [H3N+—CH2—COOH]Cl¯ (образование солей по аминогруппе) 2. H2N—CH2—COOH + NaOH → H2N—CH2—COO¯Na+ + H2O (образование солей) 3. 
(образование сложного эфира) 4. 
(ацилирование) 5. +NH3—CH2—COO¯ + 3CH3I →—HI→ (CH3)3N+—CH2—COO¯ – бетаин аминоуксусной кислоты (алкилирование) 6. 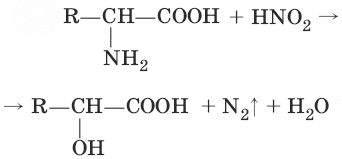
(взаимодействие с азотистой кислотой) 7. nH2N—(CH2)5—COOH → (—HN—(CH2)5—CO—)n+ nH2O (получение капрона) 15. Углеводы. Моносахариды. Олигосахариды. ПолисахаридыУглеводы (сахара) – органические соединения, имеющие сходное строение и свойства, состав большинства которых отражает формула Сх(Н2O)y, где х, у ≥ 3. Классификация: 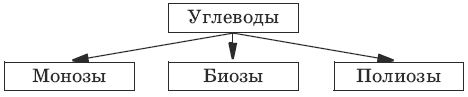
Моносахариды не гидролизуются с образованием более простых углеводов. Олиго-и полисахариды расщепляются при кислом гидролизе до моносахаридов. Общеизвестные представители: глюкоза (виноградный сахар) С6Н12O6, сахароза (тростниковый, свекловичный сахар) С12Н22О11, крахмал и целлюлоза [С6Н10О5]n. Способы получения1. mCO2 + nН2O →hv, хлорофилл→ Cm(H2O)n (углеводы)+ mO2 (получение при фотосинтезе) углеводы: С6Н12O6 + 6O2 → 6CO2 + 6Н2O + 2920 кДж (метаболизм: глюкоза окисляется с выделением большого количества энергии в живом организме в процессе метаболизма) 2. 6nCO2 + 5nН2O →hv, хлорофилл→ (С6Н10О5)n + 6nO2 (получение крахмала или целлюлозы) Химические свойстваМоносахриды. Все монозы в кристаллическом состоянии имеют циклическое строение (α– или β-). При растворении в воде циклический полуацеталь разрушается, превращаясь в линейную (оксо-) форму. 
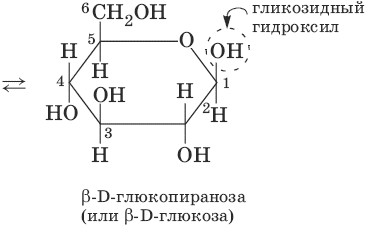
Химические свойства моносахаридов обусловлены наличием в молекуле функциональных групп трех видов (карбонила, спиртовых гидроксилов и гликозидного (полуацетального) гидроксила). 1. С5Н11O5—CHO (глюкоза) + Ag2O →NH3→ CH2OH—(CHOH)4—COOH (глюконовая кислота) + 2Ag (окисление) 2. С5Н11O5—CHO (глюкоза) + [Н] → CH2OH—(CHOH)4—CH2OH(сорбит)(восстановление) 3. а) 
(моноалкилирование) б) 
(полиалкилирование) 4. 
5. Важнейшим свойством моносахаридов является их ферментативное брожение, т. е. распад молекул на осколки под действием различных ферментов. Брожению подвергаются в основном гексозы в присутствии ферментов, выделяемых дрожжевыми грибками, бактериями или плесневыми грибками. В зависимости от природы действующего фермента различают реакции следующих видов: а) С6Н12O6 → 2С2Н5OH + 2CO2 (спиртовое брожение); б) С6Н12O6 → 2CH3—CH(OH)—COOH (молочнокислое брожение); в) С6Н12O6 → С3Н7COOH + 2CO2 + 2Н2O (маслянокислое брожение); г) С6Н12O6 + O2 → HOOC—CH2—С(OH)(COOH)—CH2—COOH + 2Н2O (лимоннокислое брожение); д) 2С6Н12O6 → С4Н9OH + CH3—CO—CH3 + 5CO2 + 4Н2 (ацетон-бутанольное брожение). Дисахариды. Дисахариды – углеводы, молекулы которых состоят из двух остатков моносахаридов, соединенных друг с другом за счет взаимодействия гидроксильных групп (двух полуацетальных или одной полуацетальной и одной спиртовой). Отсутствие или наличие гликозидного (полуацетального) гидроксила отражается на свойствах дисахаридов. Биозы делятся на две группы: восстанавливающие и невосстанавливающие. Восстанавливающие биозы способны проявлять свойства восстановителей и при взаимодействии с аммиачным раствором серебра окисляться до соответствующих кислот, содержат в своей структуре гликозидный гидроксил, связь между монозами – гликозид-гликозная. Схема образования восстанавливающих биоз на примере мальтозы: 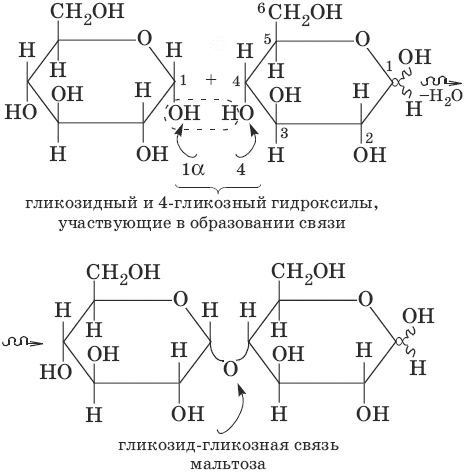
Для дисахаридов характерна реакция гидролиза, в результате которой образуются две молекулы моносахаридов: 
Примером наиболее распространенных в природе дисахаридов является сахароза (свекловичный или тростниковый сахар). Молекула сахарозы состоит из остатков α-D-глюкопиранозы и β-D-фруктофуранозы, соединенных друг с другом за счет взаимодействия полуацетальных (гликозидных) гидроксилов. Биозы этого типа не проявляют восстанавливающих свойств, так как не содержат в своей структуре гликозидного гидроксила, связь между монозами – гликозид-гликозидная. Подобные дисахариды называют невосстанавливающими, т. е. не способными окисляться. Схема образования сахарозы: 
Инверсия сахарозы. При кислом гидролизе (+)сахарозы или при действии инвертазы образуются равные количества D(+)глюкозы и D(-)фруктозы. Гидролиз сопровождается изменением знака удельного угла вращения [α] с положительного на отрицательный, поэтому процесс называют инверсией, а смесь D(+)глюкозы и D(-)фруктозы – инвертным сахаром. 
Полисахариды (полиозы). Полисахариды – природные высокомолекулярные углеводы, макромолекулы которых состоят из остатков моносахаридов. Основные представители: крахмал и целлюлоза, которые построены из остатков одного моносахарида – D-глюкозы. Крахмал и целлюлоза имеют одинаковую молекулярную формулу: (С6Н10О5)n, но различные свойства. Это объясняется особенностями их пространственного строения. Крахмал состоит из остатков α-D-глюкозы, а целлюлоза – из β-D-глюкозы. Крахмал – резервный полисахарид растений, накапливается в виде зерен в клетках семян, луковиц, листьев, стеблей, представляет собой белое аморфное вещество, нерастворимое в холодной воде. Крахмал – смесь амилозы и амилопектина, которые построены из остатков α-D-глюкопиранозы. Амилоза – линейный полисахарид, связь между остатками D-глюкозы 1α-4. Форма цепи – спиралевидная, один виток спирали содержит 6 остатков D-глюкозы. Содержание амилозы в крахмале – 15–25 %. 
амилоза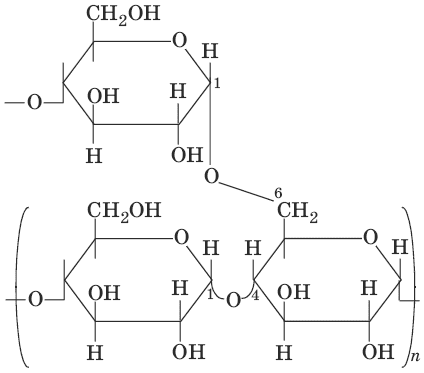
амилопектинАмилопектин – разветвленный полисахарид, связи между остатками D-глюкозы – 1α-4 и 1α-6. Содержание амилопектина в крахмале 75–85 %. Характеристика химических свойств1. Образование простых и сложных эфиров (аналогично биозам). 2. Качественная реакция – окрашивание при добавлении иода: для амилозы – в синий цвет, для амилопектина – в красный цвет. 3. Кислый гидролиз крахмала: крахмал → декстрины → мальтоза → α-D-глюкоза. Целлюлоза. Структурный полисахарид растений, построен из остатков β-D-глюкопиранозы, характер соединения 1β-4. Содержание целлюлозы, например, в хлопчатнике – 90–99 %, в лиственных породах – 40–50 %. Этот биополимер обладает большой механической прочностью и выполняет роль опорного материала растений, образуя стенки растительных клеток. Характеристика химических свойств1. Кислый гидролиз (осахаривание): целлюлоза → целлобиоза → β-D-глюкоза. 2. Образование сложных эфиров a) 

Из растворов ацетата целлюлозы в ацетоне изготавливают ацетатное волокно. б) 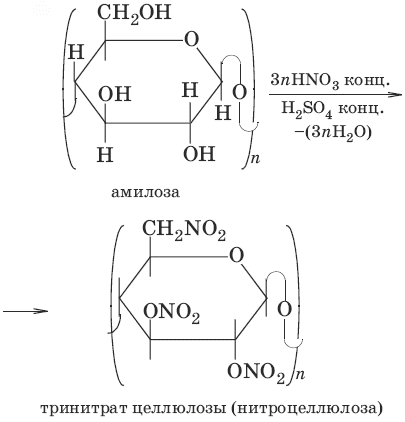
Нитроцеллюлоза взрывоопасна, составляет основу бездымного пороха. Пироксилин – смесь ди– и тринитратов целлюлозы – используют для изготовления целлулоида, коллодия, фотопленок, лаков.
Внимание !У вас нет прав для чтения и добавления комментариев. Пожалуйста авторизуйтесь или зарегистрируйтесь.Добавление комментария Есть что сказать? Пишите, нам всегда интересно знать Ваше мнение! Все вопросы по поводу данной новости оставляйте здесь, администрация и другие пользователи портала постараются Вам помочь. Пожалуйста, пишите комментарии без орфографических и пунктуационных ошибок. |
ЧасыОнлайнОнлайн всего: 1 Гостей: 1 Пользователей: 0
|
||||






 Всего: 91
Всего: 91  Новых за месяц: 0
Новых за месяц: 0