Добро пожаловать на наш портал
На нашем сайте ежедневно публикуются десятки качественных и свежих материалов, которые Вы можете скачать абсолютно бесплатно. Рекомендуем Вам добавить Наш сайт в закладки, а также подписаться на RSS ленту, чтобы не пропускать интересных новостей.




Перевести страницуМини-чатОпрос |
II. Неорганическая химия 1 часть
Просмотров: 1991
18.01.2012
II. НЕОРГАНИЧЕСКАЯ ХИМИЯ1. Основные классы неорганических соединений
1.1. ОксидыОксиды – сложные вещества, состоящие из атомов кислорода в степени окисления -2 и атомов другого элемента. Номенклатура: Fe2O3 – оксид железа(III), Cl2O – оксид хлора(I). Классификация оксидовНесолеобразующие (безразличные) оксиды: CO, SiO, NO, N2O. Солеобразующие оксиды: основные – оксиды металлов в степени окисления +1, +2, амфотерные – оксиды металлов в степени окисления +2, +3, +4, кислотные – оксиды металлов в степени окисления +5, +6, +7 и оксиды неметаллов в степени окисления +1 – +7. Получение оксидовГорение простых веществ: С + O2 = CO2 2Са + O2 = 2СаО Горение (обжиг) сложных веществ: CH4 + 2O2 = CO2 + 2Н2O 4FeS2 + 11O2 = 2Fe2O3 + 8SO2 Разложение сложных веществ: CaCO3 →t→ СаО + CO2 2Fe(OH)3 →t→ Fe2O3 + ЗН2O Химические свойства оксидовОсновным оксидам (Na2O, CaO, CuO, FeO) соответствуют основания. СаО + Н2O = Са(OH)2 (растворимы оксиды металлов IA– и IIА-групп, кроме Be, Mg) CuO + Н2O ≠ (оксиды остальных металлов нерастворимы) СаО + CO2 = CaCO3 СаО + 2HCl = CaCl2 + Н2O Кислотным оксидам (CO2, Р2O5, СrO3, Mn2O7) соответствуют кислоты. SO2 + Н2O = H2SO3 (кислотные оксиды, кроме SiO2, растворимы в воде) SO2 + СаО = CaSO3 SO2 + 2NaOH = Na2SO3 + Н2O Амфотерным оксидам (ZnO, Al2O3, Cr2O3, ВеО, РЬО) соответствуют амфотерные гидроксиды. ZnO + H2O ≠ (амфотерные оксиды нерастворимы в воде) ZnO + 2HCl = ZnCl2 + Н2O ZnO + 2NaOH →t→ Na2ZnO2 + Н2O (при нагревании или сплавлении) ZnO + 2NaOH + H2O = Na2[Zn(OH)4] (в разбавленном растворе) 1.2. ОснованияОснования – сложные вещества, состоящие из атомов металла и гидроксиль-ных групп; основания – электролиты, образующие при диссоциации в качестве анионов только анионы гидроксила. Номенклатура: Fe(OH)3 – гидроксид железа(III). Классификация оснований:– растворимые (щелочи) NaOH, KOH; – нерастворимые Fe(OH)2, Mg(OH)2; – амфотерные Zn(OH)2, Al(OH)3, Ве(OH)2, Сr(OH)3; – однокислотные NaOH, KOH; – двухкислотные Ва(OH)2, Zn(OH)2; – трехкислотные Al(OH)3, Сr(OH)3. Получение основанийПолучение щелочей: 2Na + 2Н2O = 2NaOH + Н2 Na2O + Н2O = 2NaOH Получение нерастворимых и амфотер-ных оснований: FeSO4 + 2NaOH = Fe(OH)2↓ + Na2SO4 AlCl3 + 3NaOH = Al(OH)3↓ + 3NaCl Свойства щелочей:NaOH → Na+ + OH¯ (α = 1, фенолфталеин – красный) NaOH + HCl = NaCl + H2O (реакция нейтрализации) 2NaOH + CO2 = Na2CO3 + H2O 2NaOH + Zn(OH)2 = Na2[Zn(OH)4] 2NaOH + Al2O3 →t→ 2NaAlO2 + H2O 2NaOH + CuSO4 = Cu(OH)2↓ + Na2SO4 2NaOH + Zn + 2H2O = Na2[Zn(OH)4] + H2 2NaOH + 2Al + 6H2O = 2Na[Al(OH)4] + 3H2 2NaOH + Si + H2O = Na2SiO3 + 2H2 Свойства нерастворимых оснований:Fe(OH)2 ↔ FeOH+ + OH¯ (α << 1); FeOH+ ↔ Fe2+ + OH‾ (α << 1) Fe(OH)2 + H2SO4 = FeSO4 + 2H2O Fe(OH)2 →t→ FeO + H2O Свойства амфотерных оснований:Al3++ ЗOH¯ + Н2O ↔ Al(OH)3↓ + Н2O ↔ [Al(OH)4]¯ + Н+ Al(OH)3 + ЗHCl = AlCl3 + ЗН2O Al(OH)3 + NaOH = Na[Al(OH)4] 2Al(OH)3 →t→ Al2O3 + ЗН2O 1.3. КислотыКислоты – сложные вещества, состоящие из атомов водорода и кислотного остатка; кислоты – электролиты, образующие при диссоциации в качестве катионов только катионы водорода. Номенклатура кислот и кислотных остатков: 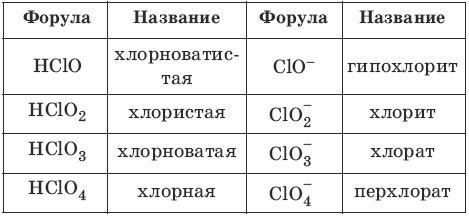

Классификация кислот:– одноосновные HCl – двухосновные H2S – трехосновные Н3PO4 – кислородсодержащие HNO3 – бескислородные HCl Получение кислотCO2 + Н2O = Н2CO3 (кроме SiO2) Na2SiO3 + H2SO4 = Na2SO4 + H2SiO3↓ H2 + Cl2 = 2HCl Химические свойства кислотHCl → H+ + CI¯ (α =1) (лакмус – красный) CH3COOH ↔ CH3COO¯ + H+ (α << 1) Fe + 2HCl = FeCl2 + H2 (металл в ряду напряжений до Н) Cu + HCl ≠ (не идет, металл в ряду напряжений после Н) 2HCl + CuO = CuCl2 + Н2O 2HCl + Cu(OH)2 = CuCl2 + 2Н2O 2HCl + ZnO = ZnCl2 + Н2O 3HCl + Al(OH)3 = AlCl3 + 3Н2O 2HCl + Na2CO3 = 2NaCl + H2O + CO2↑ (выделяется газ) HCl + AgNO3 = AgCl↓ + HNO3 (образуется осадок) 1.4. СолиСоли – сложные вещества, состоящие из атомов металла и кислотного остатка. Соли – электролиты, образующие при диссоциации катионы металла или аммония и анионы кислотного остатка. Номенклатура солейNa2HPO4 – гидрофосфат натрия Са(Н2PO4)2 – дигидрофосфат кальция AlOHSO4 – гидроксид сульфат алюминия KMgF3 – фторид калия магния NaCl • NaF – фторид хлорид натрия NaNH4HPO4 – гидрофосфат аммония натрия Na2[Zn(OH)4] – тетрагидроксоцинкат натрия Классификация солей– средние – MgCl2, Na3PO4 – кислые – Na2HPO4, Ca(H2PO4)2 – основные – MgOHCl, (Al(OH)2)2SO4 – смешанные – NaCl • NaF, CaBrCl – двойные – KMgF3, KAl(SO4)2 – комплексные – Na2[Zn(OH)4], K3[Cr(OH)6] – кристаллогидраты – CuSO4 • 5H2O Получение солей (на примере получения CuS04)Cu + 2H2SO4 конц = CuSO4 + SO2 + 2H2O Cu + 2AgNO3 = Cu(NO3)2 + 2Ag CuO + H2SO4 = CuSO4 + H2O CuO + SO3 = CuSO4 Cu(OH)2 + H2SO4 = CuSO4 + 2H2O CuCO3 + H2SO4 = CuSO4 + H2O + CO2 CuCl2 + Ag2SO4 = CuSO4 + 2AgCl↓ Химические свойства солейNaHCO3 → Na+ + HCO3¯ (α = 1) HCO3¯ ↔ H+ + CO32- (α << 1) MgOHCl → MgOH+ + CI¯ (α = 1) MgOH+ ↔ Mg2+ + OH¯ (α << 1) NaHSO4 → Na+ + Н+ + SO4¯ (α = 1) CuSO4 + Fe = Cu + FeSO4 (Fe до Cu в ряду напряжений) Pb + ZnCl2 ≠ (Pb после Zn в ряду напряжений) CuSO4 + 2NaOH = Cu(OH)2↓ + Na2SO4 (осадок) CuSO4 + H2S = CuS↓ + H2SO4 (осадок) CuSO4 + BaCl2 = BaSO4↓ + CuCl2 (осадок) Разложение некоторых солей при нагреванииCa(HCO3)2 →t→ CaCO3↓ + H2O + CO2 (при кипячении воды) CaCO3 →t→ CaO + CO2 (роме устойчивых карбонатов щелочных металлов) 2NaNO3 →t→ 2NaNO2 + O2 (металл до Mg в ряду напряжений) 2Pb(NO3)2 →t→ 2РbO + 4NO2 + O2 (металл от Mg до Cu в ряду напряжений) 2AgNO3 →t→ 2Ag + 2NO2 + O2 (металл после Cu в ряду напряжений) NH4Cl →t→ NH3 + HCl (при охлаждении идет в противоположном направлении) NH4NO3 →t→ N2O + 2Н2O (получение «веселящего» газа) NH4NO2 →t→ N2 + 2H2O (получение азота в лаборатории) (NH4)2Cr2O7 →t→ N2 + Cr2O3 + 4Н2O (реакция «вулкан») 4KClO3 →400 °C→ KCl + 3KClO4 2KClO3 →t, MnO4→ 2KCl + 3O2 2КMnO4 →t→ К2MnO4 + MnO2 + O2 Связь между классами соединенийМеталл ↔ основный оксид ↔ основание ↔ соль Неметалл ↔ кислотный оксид ↔ кислота ↔ соль 2. IА-группаЩелочные металлы Li, Na, К, Rb, Cs, Fr.Атомы этих элементов имеют электронную формулу ns1. Они являются сильными восстановителями. Их активность растет от лития к цезию. Для них характерна степень окисления +1. В природе щелочные металлы находятся в виде хлоридов, сульфатов, карбонатов, силикатов и т. д. Щелочные металлы мягкие, легко режутся ножом, на свежем срезе имеют серебристую окраску. Все они легкие и легкоплавкие металлы с хорошей электропроводностью. В парообразном состоянии атомы щелочных металлов образуют молекулы Э2, например Na2. 2.1. Получение и химические свойства щелочных металловПолучение 2NaCl →электролиз расплава→ 2Na + Cl2 KCl + Na →800ºС→ К + NaCl Горение в кислороде 4Li + O2 →t→ 2Li2O 2Na + O2 →t→ Na2O2 К + O2 →t→ KO2 Реакции с другими неметаллами 2Na + Cl2 = 2NaCl 2Na + H2 →t→ 2NaH 2К + S = K2S 6Li + N2 = 2Li3N Реакции с водой и разбавленными кислотами 2Na + 2Н2O = 2NaOH + H2↑ 2Na + 2HCl = 2NaCl + H2↑ 2.2. Получение и химические свойства соединений щелочных металловОксиды. Оксиды щелочных металлов являются активными основными оксидами. 4Li + O2 →t→ 2Li2O Na2O2 + 2Na →t→ 2Na2O Na2O + Н2O = 2NaOH Na2O + CO2 = Na2CO3 Na2O(тв) + Al2O3(тв) →t→ 2NaAlO2 Na2O + 2HCl = 2NaCl + H2O Гидроксиды. Гидроксиды щелочных металлов – растворимые основания, щелочи. Их степень диссоциации увеличивается от LiOH к CsOH. NaOH → Na+ + OH¯ (α ≈ 1) 2NaOH + CO2 = Na2CO3 + Н2O 2NaOH + H2SO4 = Na2SO4 + 2H2O 2NaOH + Zn + 2H2O = Na2[Zn(OH)4] + H2 2NaOH + ZnO →t→ Na2ZnO2 + H2O NaOH + Al(OH)3 = Na[Al(OH)4] 3NaOH + FeCl3 = Fe(OH)3↓ + 3NaCl Гидриды. Гидриды щелочных металлов – восстановители. NaH + Н2O = NaOH + Н2 NaH + HCl = NaCl + H2 NaH + Cl2 →t→ NaCl + HCl Пероксиды и надпероксиды. Являются окислителями. Na2O2 + 2Н2O = 2NaOH + H2O2 Na2O2 + 2HCl = 2NaCl + H2O2 2Na2O2 + 2CO2 = 2Na2CO3 + O2 Na2O2 + 2KI + 2H2SO4 = Na2SO4 + I2 + K2SO4 + 2H2O Na2O2 + CO →t→ Na2CO3 2KO2 + 2H2O = 2KOH + H2O2 + O2 2KO2 + CO →t→ K2CO3 + O2 Соли. Хорошо растворяются в воде. Соли лития окрашивают пламя горелки в карминово-красный цвет, соли натрия – в желтый цвет, соли калия – в светло-фиолетовый цвет. Соли щелочных металлов со слабыми кислотами гидролизуются, создавая щелочную среду. Na2CO3 + H2O ↔ NaHCO3 + NaOH 2Na+ + CO32- + H2O ↔ CO3¯ + OH¯ + 2Na+ CO32- + H2O ↔ CO3¯ + OH¯ 3. IIА-группаЭлементы IIА-группы имеют электронную формулу ns2. Все они являются металлами, сильными восстановителями, несколько менее активными, чем щелочные металлы. Для них характерна степень окисления +2 и валентность II. Щелочноземельные металлы: Са, Sr, Ba, Ra. В природе элементы IIА-группы находятся в виде солей: сульфатов, карбонатов, фосфатов, силикатов. Элементы IIА-группы представляют собой легкие серебристые металлы, более твердые, чем щелочные металлы. 3.1. Получение и химические свойства простых веществЭлементы IIА-группы – менее активные восстановители, чем щелочные металлы. Их восстановительные свойства увеличиваются от бериллия к радию. Кислород воздуха окисляет Са, Sr, Ba, Ra при обычной температуре. Mg и Be покрыты оксидными пленками и окисляются кислородом только при нагревании: CaCl2 →электролиз расплава→ Са + Cl2 2Са + O2 →t→ 2СаО 2Mg + O2 →t→ 2MgO Са + Cl2 = CaCl2 Са + Н2 →t→ СаН2 Са + 2С →t→ СаС2 Са + 2Н2O = Са(OH)2 + H2↑ Mg + 2Н2O(хол.) ≠ Mg + 2Н2O(гор.) →t→ Mg(OH)2 + H2↑ Mg + 2HCl = MgCl2 + H2↑ 4Mg + 10HNO3(pазб.) = 4Mg(NO3)2 + NH4NO3 + 3H2O 3.2. Получение и химические свойства соединенийОксиды Оксид бериллия – амфотерный оксид. Оксид магния – нерастворимый основный оксид. Оксид кальция – растворимый основный оксид. CaCO3 →t→ СаО + CO2 2Са + O2 →t→ 2СаО ВеО + Н2O ≠ ВеО + 2HCl = ВeCl2 + Н2O ВеО + 2NaOH →t→ Na2BeO2 + Н2O MgO + Н2O ≠ MgO + 2HCl = MgCl2 + Н2O MgO + NaOH ≠ СаО + Н2O = Са(OH)2 СаО + CO2 = CaCO3 СаО + 2HCl = CaCl2 + Н2O Гидроксиды Гидроксид бериллия – амфотерное основание. Гидроксид магния – нерастворимое основание. Гидроксиды щелочноземельных металлов – щелочи. Ве(OH)2↓ + 2HCl = ВeCl2 + 2Н2O Ве(OH)2↓ + 2NaOH = Na2[Be(OH)4] Ве(OH)2 →t→ ВеО + Н2O Mg(OH)2↓+ 2HCl = MgCl2 + 2Н2O Mg(OH)2↓ + NaOH ≠ Mg(OH)2 →t→ MgO + H2O Ba(OH)2 + 2HCl = BaCl2 + 2H2O Ba(OH)2 + CO2 = BaCO3↓ + H2O Ba(OH)2 + H2SO4 = BaSO4↓ + 2H2O Гидриды Имеют восстановительные свойства. СаН2 + 2Н2O = Са(OH)2 + 2Н2 СаН2 + 2HCl = CaCl2 + 2Н2 Пероксиды ВaO2 + 2Н2O = Ва(OH)2 + Н2O2 ВaO2 + 2HCl = ВaCl2 + Н2O2 2ВaO2 + 2CO2 = 2ВaCO3 + O2 Соли Содержание ионов Са2+ и Mg2+ обуславливает жесткость воды: временную, если есть гидрокарбонаты Са и Mg, и постоянную, если в воде есть хлориды или сульфаты Са и Mg. CaCl2 + Na2CO3 = CaCO3↓ + 2NaCl Са(HCO3)2 + Са(OH)2 = 2CaCO3↓ + 2Н2O Са(HCO3)2 →t→ CaCO3↓ + Н2O + CO2↑ CaCO3↓ + H2O + CO2 = Са(HCO3)2 CaCO3 + 2HCl = CaCl2 + Н2O + CO2↑ 4. IIIА-группаЭлементы IIIА-группы имеют электронную формулу ns2np1. Они являются значительно менее активными восстановителями, чем щелочноземельные металлы. Для них характерна степень окисления +3 и валентность III. В группе сверху вниз возрастают металлические свойства элементов, увеличиваются восстановительные свойства их атомов. Увеличиваются основные свойства гидроксидов и уменьшаются их кислотные свойства. 
Соединения Тl3+ являются сильными окислителями и восстанавливаются до соединений Тl+. 4.1. Химические свойства бора и его соединений4В + 3O2 →t→ 2В2O3 В2O3 + ЗН2O = 2Н3ВO3 Н3ВO3 →t→ HBO2 →t→ Н2В4O7 →t→ В2O3 4Н3ВO3 + 2NaOH = Na2B4O7 + 7H2O Na2B4O7 + H2SO4 + 5H2O = Na2SO4 + 4Н3ВO3 B(OH)3 + 3C2H5OH →H2SO4(конц.)→ B(OC2H5)3 + 3H2O 4.2. Химические свойства алюминия и его соединений2Al2O3 →электролиз расплава→ 4Al + 3O2 4Al + 3O2 = 2Al2O3 (металл покрыт оксидной пленкой) 2Al + 6Н2O = 2Al(OH)3 + ЗН2 (без оксидной пленки) 2Al + 6HCl = 2AlCl3 + ЗН2 2Al + 2NaOH + 6Н2O = 2Na[Al(OH)4] + ЗН2 8Al + 3Fe3O4 →t→ 9Fe + 4Al2O3 Оксид алюминия – амфотерный оксид Al2O3 + Н2O ≠ Al2O3 + 6HCl = 2AlCl3 + ЗН2O Al2O3 + 2NaOH →t→ 2NaAlO2 + Н2O Гидроксид алюминия – амфотерный гидроксид. AlCl3 + 3NH4OH = Al(OH)3↓ + 3NH4Cl AlCl3 + 3NaOH = Al(OH)3↓ + 3NaCl Al(OH)3↓ + NaOH = Na[Al(OH)4] Al(OH)3↓ + 3HCl = AlCl3 + 3H2O 2Al(OH)3 →t→ Al2O3 + 3H2O Соли алюминия гидролизуются. Некоторые из них (Al2S3, Al2(CO3)3) полностью разлагаются водой. Al2S3 + 6Н2O = 2Al(OH)3↓ + 3H2S↑ Al2(CO3)3 + ЗН2O = 2Al(OH)3↓+ 3CO2↑ 5. IVA-группаЭлементы IVA-группы имеют электронную формулу ns2np2. Углерод и кремний являются неметаллами, германий, олово, свинец – металлами. Для элементов характерны степени окисления +4, +2, 0, -4 и валентность IV. В возбужденном состоянии атомы имеют конфигурацию ns1nps, в этом состоянии для них характерна sp3-гибридизация. 5.1. Свойства углерода и его соединенийХарактерные степени окисления углерода, электронные формулы соответствующих ионов, химические свойства и примеры соединений приведены в таблице. 
Свойства углерода 2С + O2(недостаток) →t→ 2CO С + O2(избыток) →t→ CO2 С + CO2 →t→ 2CO С + CuO →t→ Cu + CO 4С + Fe3O4 →t→ 3Fe + 4CO ЗС + СаО →t→ СаС2 + CO 2С + Са →t→ СаС2 ЗС + 4Al →t→ Al4С3 С + 4НNO3(конц.) →t→ CO2 + 4NO2 + 2Н2O Свойства оксида углерода (II) – угарного газа 2CO + O2 →t→ 2CO2 ЗCO + Fe2O3 →t→ 2Fe + ЗCO2 CO + CuO →t→ Cu + CO2 CO + H2O →t, катализатор→ CO2 + Н2 CO + NaOH →t, p→ HCOONa Свойства оксида углерода(IV) – углекислого газа CaCO3 + 2HCl = CaCl2 + Н2O + CO2↑ CaCO3 →t→ СаО + CO2 CO2 + Н2O ↔ Н2CO3 ↔ H+ + HCO3¯ ↔ 2Н+ + CO32- CO2 + Са(OH)2 = CaCO3↓ + Н2O CO2 + Н2O + CaCO3↓ = Са(HCO3)2 CO2 + 2Mg →t→ С + 2MgO Свойства карбонатов и гидрокарбонатов NaOH + CO2 = NaHCO3 2NaOH + CO2 = Na2CO3 + H2O Са(HCO3)2 →100 °C→ CaCO3↓ + Н2O + CO2↑ CaCO3 →1000 °C→ СаО + CO2 2NaHCO3 →t→ Na2CO3+ Н2O + CO2↑ NaHCO3+ CH3COOH = CH3COONa + Н2O + CO2↑ CaCO3 + Н2O + CO2 = Са(HCO3)2 Са(HCO3)2 + Са(OH)2 = CaCO3↓ + 2Н2O Na2CO3 + H2O ↔ NaHCO3 + NaOH NaHCO3 + (Н2O) ↔ NaOH + (Н2O) + CO2 Свойства карбидов СаС2 + 2Н2O = Са(OH)2 + С2Н2 Al4С3 + 12HCl = 4AlCl3 + ЗCH4 5.2. Получение и свойства кремния и его соединенийПростое вещество SiO2 + 2Mg →t→ Si + 2MgO Si + O2 →t→ SiO2 Si + 2F2 = SiF4↑ Si + 2Mg →t→ Mg2Si Si + 2KOH + 2H2O = K2SiO3 + 2H2 Силан SiH4 Mg2Si + 4HCl = 2MgCl2 + SiH4↑ SiH4 + 2O2 = SiO2 + 2Н2O (самовоспламенение на воздухе) Оксид кремния (IV) SiO2 + H2O ≠ SiO2 + 2NaOH →t, сплавление→ Na2SiO3 + Н2O SiO2 + 6HF = H2[SiF6] + 2H2O Кремниевая кислота и силикаты. Кремниевая кислота имеет полимерное строение и состав xSiO2 • yH2O. H2SiO3 – условная формула, такого соединения не выделено. Na2SiO3 + 2HCl = H2SiO3↓ + 2NaCl Na2SiO3 + 2Н2O + 2CO2 = 2NaHCO3 + H2SiO3↓ H2SiO3 →t→ SiO2 + H 2O 5.3. Получение и свойства соединений олова и свинцаГидроксиды олова и свинца имеют амфо-терные свойства. При этом в степени окисления элемента +2 в гидроксидах преобладают основные свойства, а в степени окисления +4 – кислотные. Соединения Sn2+ имеют восстановительные свойства, а соединения РЬ4+ – окислительные: SnCl2 + 2NaOH = Sn(OH)2↓ + 2NaCl Sn(OH)2↓ + 2HCl = SnCl2 + 2H2O Sn(OH)2↓ + 2NaOH = Na2[Sn(OH)4] SnCl4 + 4NH4OH = H2SnO3↓ + 4NH4Cl + H2O H2SnO3↓ + 2NaOH + H2O = Na2[Sn(OH)6] H2SnO3↓ + 4HCl = SnCl4 + 3H2O SnCl2 + 2FeCl3 = 2FeCl2 + SnCl4 PbO2 + 4HCl = PbCl2 + Cl2↑ + 2H2O
Внимание !У вас нет прав для чтения и добавления комментариев. Пожалуйста авторизуйтесь или зарегистрируйтесь.Добавление комментария Есть что сказать? Пишите, нам всегда интересно знать Ваше мнение! Все вопросы по поводу данной новости оставляйте здесь, администрация и другие пользователи портала постараются Вам помочь. Пожалуйста, пишите комментарии без орфографических и пунктуационных ошибок. |
ЧасыОнлайнОнлайн всего: 5 Гостей: 5 Пользователей: 0
|
||||






 Всего: 91
Всего: 91  Новых за месяц: 0
Новых за месяц: 0