Добро пожаловать на наш портал
На нашем сайте ежедневно публикуются десятки качественных и свежих материалов, которые Вы можете скачать абсолютно бесплатно. Рекомендуем Вам добавить Наш сайт в закладки, а также подписаться на RSS ленту, чтобы не пропускать интересных новостей.




Перевести страницуМини-чатОпрос |
I. Общая химия 2 часть
Просмотров: 737
18.01.2012
5. Окислительно-восстановительные реакцииОкислительно-восстановите льные реакции – реакции, которые идут с изменением степеней окисления элементов. Окисление – процесс отдачи электронов. Восстановление – процесс присоединения электронов. Окислитель – атом, молекула или ион, который принимает электроны. Восстановитель – атом, молекула или ион, который отдает электроны. Окислители, принимая электроны, переходят в восстановленную форму: F2 [ок. ] + 2ē → 2F¯ [восст.]. Восстановители, отдавая электроны, переходят в окисленную форму: Na0 [восст. ] – 1ē → Na+ [ок.]. Равновесие между окисленной и восстановленной формами характеризуется с помощью уравнения Нернста для окислительно-восстановительного потенциала: 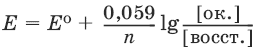
где Е0 – стандартное значение окислительно-восстановительного потенциала; n – число переданных электронов; [восст. ] и [ок. ] – молярные концентрации соединения в восстановленной и окисленной формах соответственно. Величины стандартных электродных потенциалов Е0 приведены в таблицах и характеризуют окислительные и восстановительные свойства соединений: чем поло-жительнее величина Е0, тем сильнее окислительные свойства, и чем отрицательнее значение Е0, тем сильнее восстановительные свойства. Например, для F2 + 2ē ↔ 2F¯Е0 = 2,87 вольт, а для Na+ + 1ē ↔ Na0Е0 = -2,71 вольт (процесс всегда записывается для реакций восстановления). Окислительно-восстановительная реакция представляет собой совокупность двух полуреакций, окисления и восстановления, и характеризуется электродвижущей силой (э.д.с.) ΔЕ0: ΔЕ0 = ΔЕ0ок – ΔЕ0восст, где Е0ок и ΔЕ0восст – стандартные потенциалы окислителя и восстановителя для данной реакции. Э.д.с. реакции ΔЕ0 связана с изменением свободной энергии Гиббса ΔG и константой равновесия реакции К: ΔG = – nFΔЕ0 или ΔЕ = (RT/nF)lnK. Э.д.с. реакции при нестандартных концентрациях ΔЕ равна: ΔЕ = ΔЕ0 – (RT/nF) × IgK или ΔЕ = ΔЕ0 – (0,059/n)lgK. В случае равновесия ΔG = 0 и ΔЕ = 0, откуда ΔЕ = (0,059/n)lgK и К = 10nΔE/0,059. Для самопроизвольного протекания реакции должны выполняться соотношения: ΔG < 0 или К >> 1, которым соответствует условие ΔЕ0 > 0. Поэтому для определения возможности протекания данной окислительно-восстановительной реакции необходимо вычислить значение ΔЕ0. Если ΔЕ0 > 0, реакция идет. Если ΔЕ0 < 0, реакция не идет. Химические источники токаГальванические элементы – устройства, преобразующие энергию химической реакции в электрическую энергию. Гальванический элемент Даниэля состоит из цинкового и медного электродов, погруженных в растворы ZnSO4 и CuSO4 соответственно. Растворы электролитов сообщаются через пористую перегородку. При этом на цинковом электроде идет окисление: Zn → Zn2+ + 2ē, а на медном электроде – восстановление: Cu2+ + 2ē → Cu. В целом идет реакция: Zn + CuSO4 = ZnSO4 + Cu. Анод – электрод, на котором идет окисление. Катод – электрод, на котором идет восстановление. В гальванических элементах анод заряжен отрицательно, а катод – положительно. На схемах элементов металл и раствор отделены вертикальной чертой, а два раствора – двойной вертикальной чертой. Так, для реакции Zn + CuSO4 = ZnSO4 + Cu схемой гальванического элемента является запись: (-)Zn | ZnSO4 || CuSO4 | Cu(+). Электродвижущая сила (э.д.с.) реакции равна ΔЕ0 = Е0ок – Е0восст = Е0(Cu2+/Cu) – Е0(Zn2+/Zn) = 0,34 – (-0,76) = 1,10 В. Из-за потерь напряжение, создаваемое элементом, будет несколько меньше, чем ΔЕ0. Если концентрации растворов отличаются от стандартных, равных 1 моль/л, то Е0ок и Е0восст вычисляются по уравнению Нернста, а затем вычисляется э.д.с. соответствующего гальванического элемента. Сухой элемент состоит их цинкового корпуса, пасты NH4Cl с крахмалом или мукой, смеси MnO2 с графитом и графитового электрода. В ходе его работы идет реакция: Zn + 2NH4Cl + 2MnO2 = [Zn(NH3)2]Cl + 2MnOOH. Схема элемента: (-)Zn | NH4Cl | MnO2, C(+). Э.д.с. элемента – 1,5 В. Аккумуляторы. Свинцовый аккумулятор представляет собой две свинцовые пластины, погруженные в 30%-ный раствор серной кислоты и покрытые слоем нерастворимого PbSO4. При заряде аккумулятора на электродах идут процессы: PbSO4(тв) + 2ē → Рb(тв) + SO42- PbSO4(тв) + 2H2O → РbO2(тв) + 4H+ + SO42- + 2ē При разряде аккумулятора на электродах идут процессы: РЬ(тв) + SO42- → PbSO4(тв) + 2ē РbO2(тв) + 4H+ + SO42- + 2ē → PbSO4(тв) + 2Н2O Суммарную реакцию можно записать в виде: 
Для работы аккумулятор нуждается в регулярной зарядке и контроле концентрации серной кислоты, которая может несколько уменьшаться при работе аккумулятора. 6. Растворы6.1. Концентрация растворовМассовая доля вещества в растворе w равна отношению массы растворенного вещества к массе раствора: w = mв-ва/mр-ра или w = mв-вa/(V × ρ), так как mр-ра = Vp-pa × ρр-ра. Молярная концентрация с равна отношению числа молей растворенного вещества к объему раствора: с = n(моль)/V(л) или с = m/(М × V(л)). Молярная концентрация эквивалентов (нормальная или эквивалентная концентрация) сэ равна отношению числа эквивалентов растворенного вещества к объему раствора: сэ = n(моль экв.)/V(л) или сэ = m/(Мэ × V(л)). 6.2. Электролитическая диссоциацияЭлектролитическая диссоциация – распад электролита на катионы и анионы под действием полярных молекул растворителя. Степень диссоциации α – отношение концентрации диссоциированных молекул (сдисс) к общей концентрации растворенных молекул (соб): α = сдисс/соб. Электролиты можно разделить на сильные (α ~ 1) и слабые. Сильные электролиты (для них α ~ 1) – соли и основания, растворимые в воде, а также некоторые кислоты: HNO3, HCl, H2SO4, HI, HBr, HClO4 и другие. Слабые электролиты (для них α << 1) – Н2O, NH4OH, малорастворимые основания и соли и многие кислоты: HF, H2SO3, H2CO3, H2S, CH3COOH и другие. Ионные уравнения реакций. В ионных уравнениях реакций сильные электролиты записываются в виде ионов, а слабые электролиты, малорастворимые вещества и газы – в виде молекул. Например: CaCO3↓ + 2HCl = CaCl2 + Н2O + CO2↑ CaCO3↓ + 2H+ + 2Cl¯ = Са2+ + 2Cl¯ + Н2O + CO2↑ CaCO3↓ + 2Н+ = Са2+ + Н2O + CO2↑ Реакции между ионами идут в сторону образования вещества, дающего меньше ионов, т. е. в сторону более слабого электролита или менее растворимого вещества. 6.3. Диссоциация слабых электролитовПрименим закон действия масс к равновесию между ионами и молекулами в растворе слабого электролита, например уксусной кислоты: CH3COOH ↔ CH3COО¯ + Н+ 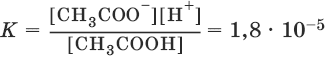
Константы равновесия реакций диссоциации называются константами диссоциации. Константы диссоциации характеризуют диссоциацию слабых электролитов: чем меньше константа, тем меньше диссоциирует слабый электролит, тем он слабее. Многоосновные кислоты диссоциируют ступенчато: Н3PO4 ↔ Н+ + Н2PO4¯ 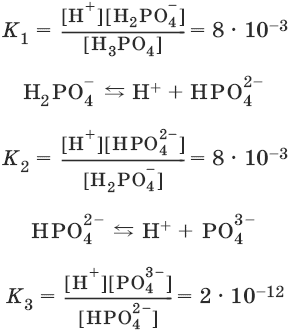
Константа равновесия суммарной реакции диссоциации равна произведению констант отдельных стадий диссоциации: Н3PO4 ↔ ЗН+ + PO43- 
Закон разбавления Оствальда: степень диссоциации слабого электролита (а) увеличивается при уменьшении его концентрации, т. е. при разбавлении: 
Влияние общего иона на диссоциацию слабого электролита: добавление общего иона уменьшает диссоциацию слабого электролита. Так, при добавлении к раствору слабого электролита CH3COOH CH3COOH ↔ CH3COО¯ + Н+ α << 1 сильного электролита, содержащего общий с CH3COOH ион, т. е. ацетат-ион, например CH3COОNa CH3COОNa ↔ CH3COО¯ + Na+ α = 1 концентрация ацетат-иона увеличивается, и равновесие диссоциации CH3COOH сдвигается влево, т. е. диссоциация кислоты уменьшается. 6.4. Диссоциация сильных электролитовАктивность иона а – концентрация иона, проявляющаяся в его свойствах. Коэффициент активности f – отношение активности иона а к концентрации с: f = а/с или а = fc. Если f = 1, то ионы свободны и не взаимодействуют между собой. Это имеет место в очень разбавленных растворах, в растворах слабых электролитов и т. д. Если f < 1, то ионы взаимодействуют между собой. Чем меньше f, тем больше взаимодействие между ионами. Коэффициент активности зависит от ионной силы раствора I: чем больше ионная сила, тем меньше коэффициент активности. Ионная сила раствора I зависит от зарядов z и концентраций с ионов: I = 0,52Σс • z2. Коэффициент активности зависит от заряда иона: чем больше заряд иона, тем меньше коэффициент активности. Математически зависимость коэффициента активности f от ионной силы I и заряда иона z записывается с помощью формулы Дебая-Хюккеля: 
Коэффициенты активности ионов можно определить с помощью следующей таблицы: 
6.5 Ионное произведение воды. Водородный показательВода – слабый электролит – диссоциирует, образуя ионы Н+ и OH¯. Эти ионы гидратированы, т. е. соединены с несколькими молекулами воды, но для простоты их записывают в негидратированной форме Н2O ↔ Н+ + OH¯. На основании закона действия масс, для этого равновесия: 
Концентрацию молекул воды [Н2O], т. е. число молей в 1 л воды, можно считать постоянной и равной [Н2O] = 1000 г/л : 18 г/моль = 55,6 моль/л. Отсюда: К • [Н2O] = К(Н2O) = [Н+] • [OH¯] = 10-14 (22°C). Ионное произведение воды – произведение концентраций [Н+] и [OH¯] – есть величина постоянная при постоянной температуре и равная 10-14 при 22°C. Ионное произведение воды увеличивается с увеличением температуры. Водородный показатель рН – отрицательный логарифм концентрации ионов водорода: рН = – lg[H+]. Аналогично: pOH = – lg[OH¯]. Логарифмирование ионного произведения воды дает: рН + рOH = 14. Величина рН характеризует реакцию среды. Если рН = 7, то [Н+] = [OH¯] – нейтральная среда. Если рН < 7, то [Н+] > [OH¯] – кислотная среда. Если рН > 7, то [Н+] < [OH¯] – щелочная среда. 6.6. Буферные растворыБуферные растворы – растворы, имеющие определенную концентрацию ионов водорода. рН этих растворов не меняется при разбавлении и мало меняется при добавлении небольших количеств кислот и щелочей. I. Раствор слабой кислоты НА, концентрация – скисл, и ее соли с сильным основанием ВА, концентрация – ссоли. Например, ацетатный буфер – раствор уксусной кислоты и ацетата натрия: CH3COOH + CHgCOONa. рН = рКкисл + lg(ссоли/скисл). II. Раствор слабого основания ВOH, концентрация – сосн, и его соли с сильной кислотой ВА, концентрация – ссоли. Например, аммиачный буфер – раствор гидроксида аммония и хлорида аммония NH4OH + NH4Cl. рН = 14 – рКосн – lg(ссоли/сосн). 6.7. Гидролиз солейГидролиз солей – взаимодействие ионов соли с водой с образованием слабого электролита. Примеры уравнений реакций гидролиза. I. Соль образована сильным основанием и слабой кислотой: Na2CO3 + H2O ↔ NaHCO3 + NaOH 2Na+ + CO32- + H2O ↔ 2Na+ + HCO3¯ + OH¯ CO32- + H2O ↔ HCO3¯ + OH¯, pH > 7, щелочная среда. По второй ступени гидролиз практически не идет. II. Соль образована слабым основанием и сильной кислотой: AlCl3 + H2O ↔ (AlOH)Cl2 + HCl Al3+ + ЗCl¯ + H2O ↔ AlOH2+ + 2Cl¯ + Н+ + Cl¯ Al3+ + H2O ↔ AlOH2+ + Н+, рН < 7. По второй ступени гидролиз идет меньше, а по третьей ступени практически не идет. III. Соль образована сильным основанием и сильной кислотой: KNO3 + H2O ≠ К+ + NO3¯ + Н2O ≠ нет гидролиза, рН ≈ 7. IV. Соль образована слабым основанием и слабой кислотой: CH3COONH4 + H2O ↔ CH3COOH + NH4OH CH3COO¯ + NH4+ + H2O ↔ CH3COOH + NH4OH, рН = 7. В ряде случаев, когда соль образована очень слабыми основаниями и кислотами, идет полный гидролиз. В таблице растворимости у таких солей символ – «разлагаются водой»: Al2S3 + 6Н2O = 2Al(OH)3↓ + 3H2S↑ Возможность полного гидролиза следует учитывать в обменных реакциях: Al2(SO4)3 + 3Na2CO3 + 3H2O = 2Al(OH)3↓ + 3Na2SO4 + 3CO2↑ Степень гидролиза h – отношение концентрации гидролизованных молекул к общей концентрации растворенных молекул. Для солей, образованных сильным основанием и слабой кислотой: 
[OH¯] = ch, рOH = – lg[OH¯], рН = 14 – рOH. Из выражения следует, что степень гидролиза h (т. е. гидролиз) увеличивается: а) с увеличением температуры, так как увеличивается K(H2O); б) с уменьшением диссоциации кислоты, образующей соль: чем слабее кислота, тем больше гидролиз; в) с разбавлением: чем меньше с, тем больше гидролиз. Для солей, образованных слабым основанием и сильной кислотой 
[Н+] = ch, рН = – lg[H+]. Для солей, образованных слабым основанием и слабой кислотой 
6.8. Протолитическая теория кислот и основанийПротолиз – процесс передачи протона. Протолиты – кислоты и основания, отдающие и принимающие протоны. Кислота – молекула или ион, способные отдавать протон. Каждой кислоте соответствует сопряженное с нею основание. Сила кислот характеризуется константой кислоты Кк. Н2CO3 + Н2O ↔ Н3O+ + HCO3¯ Кк = 4 × 10-7 [Al(Н2O)6]3+ + Н2O ↔ [Al(Н2O)5OH]2+ + Н3O+ Кк = 9 × 10-6 Основание – молекула или ион, способные принимать протон. Каждому основанию соответствует сопряженная с ним кислота. Сила оснований характеризуется константой основания К0. NH3 × Н2O (Н2O) ↔ NH4+ + OH¯ К0= 1,8 ×10-5 Амфолиты – протолиты, способные к отдаче и к присоединению протона. HCO3¯ + H2O ↔ Н3O+ + CO32- HCO3¯ – кислота. HCO3¯ + H2O ↔ Н2CO3 + OH¯ HCO3¯ – основание. Для воды: Н2O+ Н2O ↔ Н3O+ + OH¯ K(H2O) = [Н3O+][OH¯] = 10-14 и рН = – lg[H3O+]. Константы Кк и К0 для сопряженных кислот и оснований связаны между собой. НА + Н2O ↔ Н3O+ + А¯, 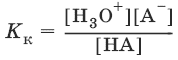
А¯ + Н2O ↔ НА + OH¯, 
Отсюда 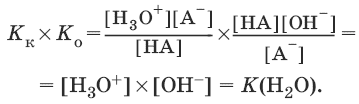
7. Константа растворимости. РастворимостьВ системе, состоящей из раствора и осадка, идут два процесса – растворение осадка и осаждение. Равенство скоростей этих двух процессов является условием равновесия. Насыщенный раствор – раствор, который находится в равновесии с осадком. Закон действия масс в применении к равновесию между осадком и раствором дает: 
Поскольку [AgClтв] = const, К • [AgClтв] = Ks(AgCl) = [Ag+] • [Cl¯]. В общем виде имеем: АmBn(тв.) ↔ mA+n + nB-m Ks(AmBn) = [А+n]m • [В-m]n. Константа растворимости Ks (или произведение растворимости ПР) – произведение концентраций ионов в насыщенном растворе малорастворимого электролита – есть величина постоянная и зависит лишь от температуры. Растворимость малорастворимого вещества s может быть выражена в молях на литр. В зависимости от величины s вещества могут быть разделены на малорастворимые – s < 10-4 моль/л, среднерастворимые – 10-4 моль/л ≤ s ≤ 10-2 моль/л и хорошо растворимые s >10-2 моль/л. Растворимость соединений связана с их произведением растворимости. 
Условие осаждения и растворения осадкаВ случае AgCl: AgCl ↔ Ag+ + Cl¯ Ks = [Ag+] • [CI¯]: а) условие равновесия между осадком и раствором: [Ag+] • [Cl¯] = Ks. б) условие осаждения: [Ag+] • [Cl¯] > Ks; в ходе осаждения концентрации ионов уменьшаются до установления равновесия; в) условие растворения осадка или существования насыщенного раствора: [Ag+] • [Cl¯] < Ks; в ходе растворения осадка концентрация ионов увеличивается до установления равновесия. 8. Координационные соединенияКоординационные (комплексные) соединения – соединения с донорно-акцеп-торной связью. Для K3[Fe(CN)6]: ионы внешней сферы – 3К+, ион внутренней сферы – [Fe(CN)6]3-, комплексообразователь – Fe3+, лиганды – 6CN¯, их дентатность – 1, координационное число – 6. Примеры комплексообразователей: Ag+, Cu2+, Hg2+, Zn2+, Ni2+, Fe3+, Pt4+ и др. Примеры лигандов: полярные молекулы Н2O, NH3, CO и анионы CN¯, Cl¯, OH¯ и др. Координационные числа: обычно 4 или 6, реже 2, 3 и др. Номенклатура. Называют сначала анион (в именительном падеже), затем катион (в родительном падеже). Названия некоторых лигандов: NH3 – аммин, Н2O – акво, CN¯ – циано, Cl¯ – хлоро, OH¯ – гидроксо. Названия координационных чисел: 2 – ди, 3 – три, 4 – тетра, 5 – пента, 6 – гекса. Указывают степень окисления комплек-сообразователя: [Ag(NH3)2]Cl – хлорид диамминсеребра(I); [Cu(NH3)4]SO4 – сульфат тетрамминмеди(II); K3[Fe(CN)6] – гексацианоферрат(III) калия. Химическая связь.Теория валентных связей предполагает гибридизацию орбиталей центрального атома. Расположение образующихся при этом гибридных орбиталей определяет геометрию комплексов. Диамагнитный комплексный ион Fe(CN)64-. Цианид-ион – донор 
Ион железа Fe2+ – акцептор – имеет формулу 3d64s04p0. С учетом диамагнитности комплекса (все электроны спарены) и координационного числа (нужны 6 свободных орбиталей) имеем d2sp3-гибридизацию: 
Комплекс диамагнитный, низкоспиновый, внутриорбитальный, стабильный (не используются внешние электроны), октаэд-рический (d2sp3-гибридизация). Парамагнитный комплексный ион FeF63-. Фторид-ион – донор. Ион железа Fe3+ – акцептор – имеет формулу 3d54s04p0. С учетом парамагнитности комплекса (электроны распарены) и координационного числа (нужны 6 свободных орбиталей) имеем sp3d2-гибридизацию: 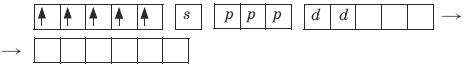
Комплекс парамагнитный, высокоспиновый, внешнеорбитальный, нестабильный (использованы внешние 4d-орбитали), октаэдрический (sp3d2-гибридизация). Диссоциация координационных соединений.Координационные соединения в растворе полностью диссоциируют на ионы внутренней и внешней сфер. [Ag(NH3)2]NO3 → Ag(NH3)2+ + NO3¯, α = 1. Ионы внутренней сферы, т. е. комплексные ионы, диссоциируют на ионы металла и лиганды, как слабые электролиты, по ступеням. 
где K1, К2, К1_2 называются константами нестойкости и характеризуют диссоциацию комплексов: чем меньше константа нестойкости, тем меньше диссоциирует комплекс, тем он устойчивее.
Внимание !У вас нет прав для чтения и добавления комментариев. Пожалуйста авторизуйтесь или зарегистрируйтесь.Добавление комментария Есть что сказать? Пишите, нам всегда интересно знать Ваше мнение! Все вопросы по поводу данной новости оставляйте здесь, администрация и другие пользователи портала постараются Вам помочь. Пожалуйста, пишите комментарии без орфографических и пунктуационных ошибок. |
ЧасыТоп пользователей
ОнлайнОнлайн всего: 1 Гостей: 1 Пользователей: 0
|
|||||||||||||||||||






 Всего: 89
Всего: 89  Новых за месяц: 0
Новых за месяц: 0