Добро пожаловать на наш портал
На нашем сайте ежедневно публикуются десятки качественных и свежих материалов, которые Вы можете скачать абсолютно бесплатно. Рекомендуем Вам добавить Наш сайт в закладки, а также подписаться на RSS ленту, чтобы не пропускать интересных новостей.




Перевести страницуМини-чатОпрос |
АРГОН
Просмотров: 776
17.01.2012
АРГОН АРГОН (от греч. argos - недеятельный; лат Argon) Ar, хим. элемент VIII гр. периодич. системы, относится к благородным газам, ат. н. 18, ат. м. 39,948. Прир. аргон состоит из изотопов с мас. ч. 36 (0,337% по объему), 38 (0,063%), 40 (99,600%), т.е., в отличие от др. легких элементов, преобладает самый тяжелый изотоп. Причина этого - концентрирование 40Аг в атмосфере в результате распада в литосфере 40К посредством захвата орбитального электрона: К + + е -> 40Аг+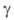 (превращ. 12% 40К). Поперечное сечение захвата тепловых нейтронов
для прир. аргона 62*10-26 м2. Конфигурация внеш. электронной
оболочки 3s23p6; энергия ионизации Аг° -> Аг+
-> Аг2+ соотв. 1520,57 и 2665,83 кДж/моль; ван-дер-ваальсов
радиус 0,192 нм, ковалентный радиус 0,095 нм.
(превращ. 12% 40К). Поперечное сечение захвата тепловых нейтронов
для прир. аргона 62*10-26 м2. Конфигурация внеш. электронной
оболочки 3s23p6; энергия ионизации Аг° -> Аг+
-> Аг2+ соотв. 1520,57 и 2665,83 кДж/моль; ван-дер-ваальсов
радиус 0,192 нм, ковалентный радиус 0,095 нм.
Аргон - самый распространенный из благородных газов элемент. В атмосфере его содержится 0,934% по объему (4*1014т), в литосфере - 4*10-6% по массе. Аргон - одноатомный газ без цвета и запаха; т. кип. 87,29 К; плотн. 0,001784
г/см3 (жидкого при 87 К - 1,40 г/см3, твердого при
40 К -1,40 г/см3); ркрит 0,4894 МПа; dкрит
0,536 г/см3; тройная точка: т-ра 83,81 К, давл. 68,9 кПа, плотн.
1,623 г/см3; Сp° 20,79 Дж/(моль*К); С водой, фенолом, гидрохиноном и ацетоном аргон образует соед. включения, а с электроотрицат. атомами в электрич. разряде или под действием пучка электронов - эксимеры (см. Благородные газы). Получают аргон в результате воздуха разделения при глубоком охлаждении. Обогащенная аргоном смесь, содержащая до 40% О2, подается на разделение в колонну. В результате получают 95%-ный аргон; степень извлечения достигает 0,75-0,80. Дальнейшая очистка от О2 осуществляется ги-дрированием в присут. платинового кат. при 333-343 К, а от N2 - низкотемпературной ректификацией. Применяется также адсорбц. метод очистки (от О2, Н2 и др. благородных газов) с использованием активного угля или молекулярных сит. Аргон может быть получен и как побочный продукт из продувочных газов в колоннах для синтеза NH3. Качественно аргон обнаруживают с помощью эмиссионного спектрального анализа; осн. характеристич. линии - 434,80 и 811,33 нм. При количеств, определении сопутствующие газы (О2, N2, H,, СО2) связываются специфич. реагентами (Са, Си, MnO, CuO, NaOH) или отделяются с помощью поглотителей (напр., водных р-ров орг. и неорг. сульфатов). Отделение от других благородных газов основано на разл. адсорбируемости их активным углем. Используются методы анализа, основанные на измерении плотности, теплопроводности и др., а также масс-спектрометрич. и хроматографич. методы. Аргон используют в кач-ве защитной среды при сварке (60-65% получаемого аргона), получении металлов и в др. металлургич. процессах (30-35%), в произ-ве полупроводниковых материалов, при хим. синтезах. Аргон применяют также как наполнитель в светотехнике (в разрядных трубках, люминесцентных лампах; 2-3%), электронике (в тиратронах и др.), ядерной технике (в ионизац. счетчиках и др.). Мировое произ-во аргона (без СССР) 5*108-5*109 м3/год. Аргон при давл. 0,4 МПа вызывает у человека оцепенение, нервно-мышечные расстройства и затуманенность мышления. Аргон поставляется, транспортируется и хранится в стальных баллонах емкостью 40 л; давление газа в баллоне до 15 МПа. Баллоны для чистого аргона окрашены в серый цвет и имеют сверху зеленую полосу, верх. часть баллона для аргона особой чистоты окрашена в белый цвет, нижняя - в черный. Аргон особой чистоты хранится также в стеклянных баллонах емкостью 2 л под давл. 0,06-0,07 МПа. Аргон открыт Дж. Рэлеем и У. Рамзаем в 1894. Внимание !У вас нет прав для чтения и добавления комментариев. Пожалуйста авторизуйтесь или зарегистрируйтесь.Добавление комментария Есть что сказать? Пишите, нам всегда интересно знать Ваше мнение! Все вопросы по поводу данной новости оставляйте здесь, администрация и другие пользователи портала постараются Вам помочь. Пожалуйста, пишите комментарии без орфографических и пунктуационных ошибок. |
ЧасыОнлайнОнлайн всего: 1 Гостей: 1 Пользователей: 0
|
||||



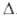 Нопл
1,17 кДж/
Нопл
1,17 кДж/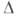 Н°исп
6,51 кДж/
Н°исп
6,51 кДж/


 Всего: 91
Всего: 91  Новых за месяц: 0
Новых за месяц: 0